
Plan Eau du Gouvernement : des solutions pour une gestion durable de l’eau
Qu’est ce que le Plan Eau lancé par le Gouvernement en mars 2023 ? Le Plan Eau lancé par le Gouvernement en mars 2023 s’inscrit dans un contexte de crise […]
Lire l'articleMerci de renseigner ce formulaire, nous vous contacterons dans les plus brefs délais.
Dans nos métiers, certaines situations nécessitent une intervention immédiate, rapide et efficace.
En savoir plus
Préambule
Contrairement à d’autres métaux usuels qui, en milieu aqueux, ne forment qu’un nombre limité de produits de corrosion, le fer peut, lui, entrainer la formation de nombreux oxydes, hydroxydes ou oxyhydroxydes, en fonction des conditions rencontrées (qualité d’eau, températures, …). Cependant, pour simplifier, il est essentiel de différencier les eaux qui contiennent de l’oxygène dissous, de celles où il est absent ou a été préalablement consommé. »
Dans une eau* contenant de l’oxygène, ce ne sont jamais des oxydes de fer qui se forment en premier, mais plutôt des hydroxydes ou oxyhydroxydes de fer, à savoir [1] :
Ces derniers, en fonction de la vitesse de corrosion, peuvent présenter différents degrés de cristallinité, allant de formes bien cristallisées à des structures amorphes.
En revanche, en absence d’oxygène dans l’eau, la maghémite γ-Fe2O3 est le seul oxyde de fer qui peut se former.
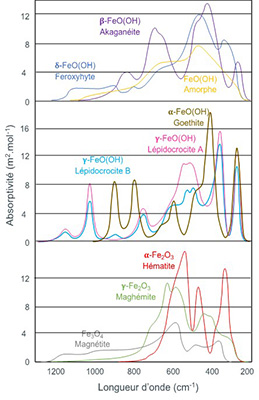
Elle est souvent confondue avec la magnétite (Fe3O4), en raison de leur couleur noire similaire et du fait que les deux sont ferromagnétiques. Parmi, les multiples techniques pour caractériser les produits de corrosion du fer, la plus «pratique» est la spectrométrie d’absorption infrarouge (Figure ci-contre) qui met en évidence des profils de spectres différents pour chaque produit de corrosion du fer [2].
Principe de la corrosion en milieu aqueux
En présence d’oxygène: Comme dans toute corrosion en milieu aqueux aéré, la corrosion commence par la réduction de l’oxygène dissous, exprimée classiquement par :
2Fe → 2Fe2+ + 4e– → (Réaction anodique)
O2 + 2H2O +4e- → 4OH- → (Réaction cathodique)
Note: La réduction des ions H+ reste possible, mais reste quasi négligeable, compte tenu de leur faible concentration pour des pH généralement supérieurs à 7.
Les ions Fe2+ vont s’oxyder immédiatement en ions Fe3+ et, leur solubilité étant extrêmement faible aux pH habituels des eaux, ils vont précipiter sous forme d’hydroxyde ferrique :
Fe3+ + 3OH– → Fe(OH)3
C’est cette hydroxyde que l’on va trouver sous les diverses formes allotropiques d’oxyhydroxydes de fer : Fe(OH)3 → FeO(OH)** + H2O
En l’absence d’oxygène (< 30 ppb), les seules réactions de réduction qui sont alors thermodynamiquement possibles, et qui peuvent donc entretenir une corrosion, sont [3] [4] :
2Fe → 2Fe2+ + 4e– (Réaction anodique)
NO3– + H2O + 2e– → NO2– + 2 OH–
NO2– + 5H2O + 6e– → NH3 + 7OH– (Réactions cathodiques)
SO42- +6H2O + 8e– → H2S + 10 OH–
les ions Fe2+ ne vont pas s’oxyder en Fe3+, ils vont précipiter sous la forme d’hydroxyde ferreux :
Fe2+ + 2OH– → Fe(OH)2
dont la déshydratation est immédiate :
2Fe(OH)2 → Fe2O3+H2O.
Le Fe2O3 formé est toujours de la maghémite (γ-Fe2O3) et jamais de l’hématite (α-Fe2O3) qui, elle, ne s’obtient que par oxydation «sèche».
Cas particulier de la magnétite.
En présence d’oxygène, pour un pH supérieur à 9, une des hypothèses serait que la gœthite formée à partir de Fe(OH)2 réagirait avec l’hydroxyde résiduel pour former de la magnétite [5] :
2α-FeOOH + Fe(OH)2 → Fe3O4 + 2H2O
En l’absence d’oxygène, il s’agit de la réaction de Schikorr :
3Fe(OH)2 → Fe3O4 + 2H2O + H2
Conclusion
Dans la pratique, en cas d’anomalie observée dans un circuit fermé, il est essentiel de s’intéresser d’abord au caractère magnétique ou non des produits de corrosion et de leur couleur. La présence de produits de couleur ocre indique généralement une corrosion en milieu aéré et témoigne de la présence d’oxyhydroxydes de fer. Une couleur noire est quant à elle indicatrice d’un circuit effectivement fermé et bien protégé par de la magnétite ou de la maghémite.
[1] Présentation CEFRACOR J. Lédion du 16/01/2020
[2] J.P. Labbé, J. Lédion, F. Hui, Infrared spectrometry for solid phase analysis: Corrosion rusts, Corrosion Science 50 (2008) 1228-1234
[3] P. Leroy, Calcium et corrosion, thèse, Université ParisV, 1991
[4] L. Legrand, P. Leroy, Prévention de la corrosion et de l’entartrage dans les réseaux de distribution d’eau, CIFEC, Paris, 1995.
[5] Y. Cudennec, A. Lecerf, Étude des mécanismes de formation des oxy-hydroxydes de fer ; hypothèses de transformations topotactiques.
Mise en pratique : Percement d’un réseau de circuit fermé.
Circuit: Réseau de Chauffage Urbain.
Traitement: ODYVAP VB 81 – ODYS NAC et ODYVAP VB 64
Appoint: 8500 m3/an.
Volume: 2000 m3.
ANALYSE
pH: 9,9
TH: 0 °f
TA: 5,5°f
TAC: 14,8°f
Chlorures: 9,9 °f
Cond.: 770 µS/cm
Fer: < 0,1 mg/L
Constat : La surface est entièrement recouverte d’une présence abondante d’oxydes de fer aimantables de couleurs noire et ocre, répartis non uniformément. Les oxydes sont difformes et de tailles différentes. Nous sommes donc vraisemblablement en présence d’un amalgame d’oxyhydoxydes de fer (ocre) de maghémite et ou de magnétite (noire).
Explication: Il s’agit d’une partie du réseau qui alterne présence et absence d’oxygène dans l’eau et donc formation alternée d’oxyhydroxydes de fer et maghémite/magnétite dont l’explication la plus probable est des carences ponctuelles et régulières en sulfites. Le dépôt formé n’est pas homogène et protecteur, il s’agit d’un mélange de différents produits de corrosion qui conjugué à la présence d’oxygène génère de la corrosion par aération différentielle avec pour conséquences l’apparition de piqûres souvent synonymes de fuites.
Solution : Il est crucial de maintenir constamment un niveau adéquat de sulfites dans l’eau en tout point du réseau, particulièrement dans les zones moins chaudes.
Alternative: Appliquer un traitement filmogène à base d’amines Filmantes et alcalinisantes pour lequel l’efficacité anti-corrosion n’est pas dépendante de la teneur en oxygène dans l’eau.
(* Excluant la vapeur, les eaux surchauffées ou géothermales – ** Généralement de la Gœthite, forme la plus stable thermodynamiquement)




Qu’est ce que le Plan Eau lancé par le Gouvernement en mars 2023 ? Le Plan Eau lancé par le Gouvernement en mars 2023 s’inscrit dans un contexte de crise […]
Lire l'article
La performance éthique de l’eau sur des km de réseau 5000 m3 d’eau pour une ville moyenne, des milliers de km de tuyaux en France.. Les réseaux de chauffage urbain […]
Lire l'article
Avec Gwladys Lemoussu, paratriathlète française participante aux Jeux Paralympiques de Paris 2024 et médaillée des Jeux Paralympiques de Rio en 2016, nous partageons l’intime conviction que, dans le traitement des […]
Lire l'article